HƯỚNG DẪN 3: ĐO ĐỘNG HỌC URE TRONG LỌC MÁU
3.1. Chúng tôi khuyến cáo mục tiêu singer pool Kt/V (spKt/V) là 1.4 mỗi buổi thận nhân tạo cho bệnh nhân điều trị ba lần mỗi tuần, với spKt/V tối thiểu 1.2. (1B)
3.2. Ở bệnh nhân có chức năng thận tự nhiên tồn dư (Kru), liều thận nhân tạo có thể giảm với điều kiện đo Kru định kỳ để tránh lọc máu không đầy đủ. (Không Phân độ)
3.3. Đối với lịch chạy thận không phải 3 lần mỗi tuần, chúng tôi đề nghị Kt/V tiêu chuẩn (stdKt/V) là 2.3 thể tích mỗi tuần với liều tối thiểu là 2.1 sử dụng phương pháp tính toán mà bao gồm sự góp phần của siêu lọc và chức năng thận tồn dư. (Không Phân độ)
GIẢI THÍCH
Liều mục tiêu (Hướng dẫn 3.1)
Hướng dẫn này không thay đổi so vớ hướng dẫn trước. Độ thanh thải chất hòa tan nhỏ được cho là công cụ đo tốt nhất của HD và tính đầy đủ của nó. Kt/V, tỷ lệ độ thanh thải ure với thể tích phân bổ ure, là phép đo tóm lược nhất và đo hiệu quả quả lọc ảnh hưởng trên tỷ lệ sống bệnh nhân và nó là phép đo ứng dụng nhiều nhất của liều lọc máu ngắt quãng. Sự khác biệt giữa liều lọc máu tối thiểu và mục tiêu là dựa trên hệ số biến thiên trong bệnh nhân ở nghiên cứu HEMO là ~ 10% và được thiết kế để hạn chế số liều điều trị mà hạ thấp xuống mức tối thiểu như đã được giải thích trong các hướng dẫn của KDOQI trước đây.7
Bằng chứng cho tầm quan trọng của thanh thải các chất hòa tan nhỏ.
Dù được thừa nhận là tương quan thô với các kết quả lâm sàng, bệnh nhân không thể sống mà không thành thải chất hòa tan nhỏ đầy đủ. Đây là một kết luận không thể chối cãi được rút ra từ sự thành công của kéo dài đời sống bằng HD, và đặc biệt ở kỷ nguyên trước đây khi màng lọc lọc được ít hoặc không với các các chất hòa tan trọng lượng phân tử lớn. Dù nồng độ mỗi độc tố được giữ lại dường như là mục tiêu đúng của liều HD (độc tính phụ thuộc nồng độ), đo bất kỳ chất hòa tan đại diện được lựa chọn bị rối loạn bởi tốc độ sản sinh (hoặc xuất hiện) của nó. Tốc độ sản sinh của một chất hòa tan có thể thay đổi và làm rối loạn từ tốc độ sản sinh của các độc tố quan trọng khác, tác dụng loại bỏ nồng độ chất hòa tan được lựa chọn khi không có tính đại diện. Tương tự, đo tốc chất hòa tan đại diện được sử dụng, trong một trạng thái cân bằng khối ổn định, đo chỉ bị ảnh hưởng bởi tốc độ sản sinh. Tuy nhiên, tỷ lệ của tốc độ loại bỏ với nồng độ chất tan, được định nghĩa là độ thanh thải chất tan, là một phéo đo chính xác của hiệu quả lọc sạch chất tan và xu hướng hằng định ở các chất tan nhỏ tương tự, độc lấp với sự thay đổi các tốc độ sản sinh và nồng độ của chất tan. Lựa chọn một chất tan làm dấu ấn để đo độ thanh thải do đó hợp lý hơn dấu ấn nồng độ bởi độ thanh thải ít bị cản trở bởi nồng độ của chất tan hoặc tốc độ sản sinh của chất tan. Chất tan đại diện lú tưởng cho đánh giá độ thanh thải nên được đo dễ dàng và di chuyển tự do bởi khuếch tan qua màng lọc và có trong các khoang của cơ thể mà không cần xắp xếp trong các khoang ở xa hoặc liên kết với các đại phân tử trong máu. Ure là một chất tan nhỏ đại diện tốt nhất hiện nay bởi sự rồi dào của nó và tân thủ chặt chẽ với các tiêu chí trên, cũng như có giá thành xét nghiệm hợp lý và thấp. Chức năng thận tự nhiên, khi còn, có thể được đo bằng độ thanh thải ure và phối hợp với độ thanh thải quả lọc để xác định được hiệu quả toàn bộ độ thanh thải các chất tan nhỏ.7
Bằng chứng cho tầm quan trọng của Thanh thải ure
Đối với HD ngắt quãng, diễn giải độ thanh thải nên gồm thời gian điều trị bệnh nhân (t) và điều chỉnh cho kích thước bệnh nhân. Được diễn giải ở dưới, phép đo tiện lợi nhất mà thỏa mãn các yêu cầu là Kt/V. Nhiều nghiên cứu quan sát và một nghiên cứu can thiệp lâm sàng đối chứng ngẫu nhiên cho thấy mỗi tương quan mạnh giữa Kt/V ure và tử vong.126-128 Một nghiên cứu can thiệp lâm sàng cho thấy không có lợi ích tỷ lệ sống ở mức độ cao của Kt/V,129, nhưng các nghiên cứu trước đây chỉ ra rõ ràng rằng chỉ số thấp hơn có liên quan mạnh đến tye lệ mắc và nên do đó phải được tránh.126,127
Phương pháp đo độ thanh thải ure
Kt/V ure là được đo phổ biến nhất sử dụng mô hình toán học của nồng độ máu ure trước và sau lọc.130,131 Phương pháp này sử dụng độ thanh thải được tích hợp hoặc trung bình trong quá trình HD và đặc hiệu người bệnh, thường được gọi là “liều HD được phân phối”
Mẫu máu trước lọc được lấy trước khi truyền nước muối sinh lý, heparin, hoặc các pha loãng khác. Mẫu máu sau lọc được lấy từ cổng lấy máu dòng vào quả lọc sử dụng phương pháp lưu lượng chậm (100 ml/phút trong 15 giây) hoặc phương pháp dừng dịch lọc (3 phút). Các phép đo đó nên được làm ít nhất hàng tháng như được khuyến cáo trong các hướng dẫn trước đây.7
Các phương pháp đã được sử dụng bằng các xét nghiệm và các cơ sở lâm sàng lọc máu ở các nước để tính toán Kt/V; các phương pháp đó bao gồm các công thức được đơn giản hóa (xem phụ lục 1), mô hình nhiều khoang, và đo độ dẫn điện online (Xem mục 5 trong Phụ lục), không phải toàn bộ tỏng số chúng là từ một chỉ số. Một ví dụ của các lỗi được sinh ra bởi các công thức đơn giản hóa được chỉ ra trong Hình 1. Dù tỷ lệ giả Ure (URR) là dễ dàng để tính và đã được sử dụng như một tiêu chuẩn để đo liều thận nhân tạo được phân phối,132 nó nên bị loại trừ dần đần với lợi ích của các phương pháo đo chính xác hơn. URR có nhiều lỗi do thay đổi ở thể tích phân bổ ure (V) và sự sản sinh ure (G) trong quá trình lọc máu và không có khả năng tích hợp với Kru của bệnh nhân trong đại diện liều lọc máu (xem dưới).
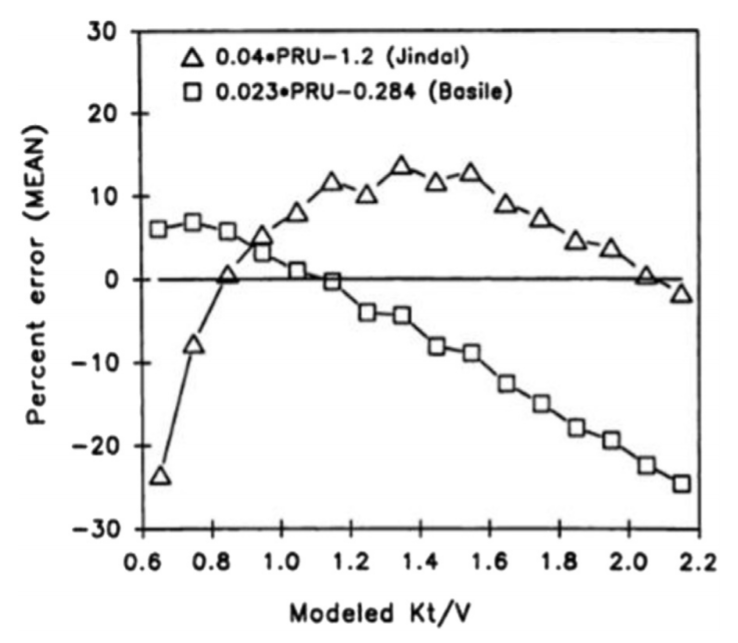
Hình 1: Lỗi hệ thống từ 2 công thức tuyến tính được sử dụng phổ biến dựa trên tỷ lệ phần trăm giảm nồng độ ure (PRU). Công thức Basile và cộng sự136 có ít lỗi hơn công thức Jindal và cộng sự137 trong khoảng bình thường nhưng nó ước tính quá mức liều trong khu vực tiêu chí Kt/V<1. Reproduced with permission of the American Society of Nephrology from Daugirdas.138
Một phương pháp tham khảo so sánh với phương pháp khác để đảm bảo tính đồng nhất và bảo vệ bệnh nhân khỏi lọc máu dưới mức hiệu quả là sẵn có trên mạng internet (www.ureakinetics.org ).133 Mô hình tham khảo này là một chương trình nguồn mở miễn phí với mục đích phi lợi nhuận và gồm có các tính toán về spKt/V, double – pool Kt/V, stdKt/V – xem dưới, và stdKt/V điều chỉnh theo diện tích da (SA-stdKt/V) (xem mục 4 trong Phụ lục).
Độ thanh thải có thể được đo trực tiếp qua quả lọc từ sự thay đổi độ dẫn điện dòng ra dịch lọc trong đáp ứng với thay đổi dạng sóng ở nồng độ dòng vào dịch lọc (xem mục 5 trong Phụ lục). các độ thanh thải độ dẫn điện phải được đo nhiều lần trong mỗi lần điều trị để thu được giá trị trung bình toàn bộ HD. Các phương pháp tính Kt/V từ đo độ dẫn điện yêu cầu hiệu chỉnh cho tái tuần hoàn tim phổi134,135 và đo độc lập với V. Ưu điểm của phương pháp này gồm dễ dàng đo, phản hồi ngay cho bác sỹ, không cần lấy máu hoặc dịch lọc để xét nghiệm, không cần vật tư (rẻ tiền), và khả năng sử dụng diện tích như một mẫu số. Nhược điểm gồm cần ước tính hoặc đo V để so sánh với Kt/V ure mô hình hóa. Ở thời điểm hiện tại, phương pháp này và các phương pháp thay thế khác để đo độ thanh thải các chất hòa tan nhỏ (như theo dõi hấp thụ UV của dịch đã sử dụng) có thể chỉ được sử dụng nếu cân bằng với tiêu chuẩn tham chiếu như đã được chú ý trên có thể được chứng minh.
Kt/V được tính sử dụng nồng độ ure nitrogen máu (BUN) sau lọc được cân bằng (eKt/V) được khuyến có bởi một số hướng dẫn như một phép đo hiệu quả lọc máu chính xác hơn.139 Những phương pháp này đo eKt/V yêu cầu đợi 30 phút sau khi đã dừng HD để lấy mẫu máu xét nghiệm sau lọc, hoặc thay thế bằng một công thức toán học dựa trên lấy mẫu máu ngay sau lọc. Dù có vẻ hợp lý, các thao tác bổ xung thêm này làm công việc trở lên phwucs tạp và không cho thấy ưu điểm hợp lý; các nghiên cứu giải thích thiếu.
Đối với HD ba buổi mỗi tuần ở bệnh nhân có độ thanh thải thận tự nhiên thấp (Kru < 2 mL/phút), spKt/V mục tiêu là 1.4 lần thể tích mỗi buổi lọc máu, liều tối thiểu là 1.2. Khuyến cáo này không thay đổi so với hướng dẫn của KDOQI trước đây.
Các điều chỉnh cho Kru (Hướng dẫn 3.2)
Tầm quan trọng của Kru
Mối tương quan giữa Kru và tỷ lệ sống bệnh nhân là mạnh và nhất quán trong nhiều nghiên cứu (Hình 2).140 Dù đóng góp một phần nhỏ cho dộ thanh thải ure, chỉ số Kru 3 mL/phút ở bệnh nhân trung bình xấp xỉ với Kt/V mỗi tuần là 1. Ngoài ra, nó đủ khả năng để kiểm soát dịch tốt hơn và lợi ích loại bỏ các chất hòa tan được lọc kém qua quả lọc bằng thận tự nhiên còn lại.141,142 Mất Kru đã được công nhận như một yếu tố góp phần làm tăng tỷ lệ tử vong đã được thấy ở bệnh nhân lọc máu nhiều lần ban đêm.
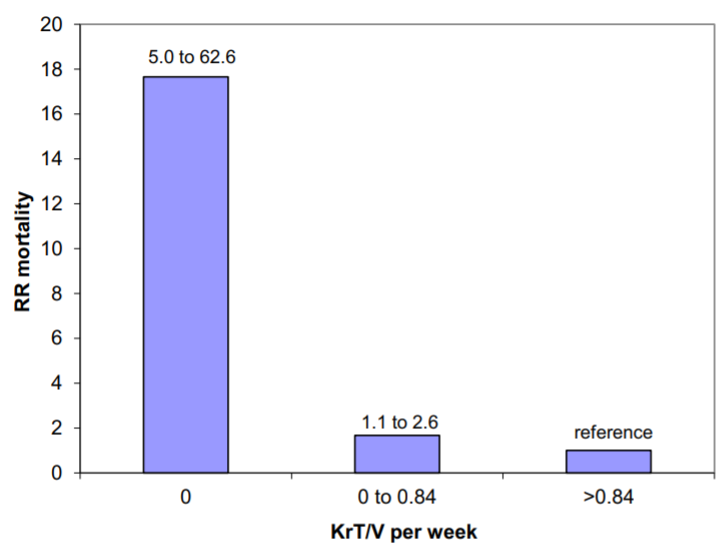
Hình 2: Dữ liệu từ Netherlands Cooperative Study cho thấy tăng rõ ràng nguy cơ tử vong ở bệnh nhân không còn chức năng thận tồn dư (KrT/V). . Data source: Termorschuizen et al.140
Phương pháp điều chỉnh bao gồm các phép đo hàng quý của Kru
Đưa Kru vào mô hình động học ure cho phép đánh giá chính xác tốc độ sản sinh ure từ quá trình dị hóa protein của bệnh nhân (PCR – protein catabolic rate). Nếu bệnh nhân có Kru đáng kể mà không đưa vào mô hình toán học, PCR sẽ bị ước tính thấp đáng kể. Công nhận rằng lấy mẫu nước tiêu là một gánh nặng mà bệnh nhân dễ từ chối, khuyến cáo đánh giá hàng quý được đưa ra. Tuy nhiên, nếu Kt/V mục tiêu được giảm đi bởi còn Kru đáng kể, và Kru thay đổi đột ngột như đã chỉ ra bởi thay đổi thể tích hoặc các nguy cơ góp phần trong quá trình điều trị nội trú, và đo không theo lịch nên được làm để tránh lọc máu không hiệu quả thời gian dài khi Kru đã mất đi. Ở những bệnh nhân đó, kê đơn điều trị lọc máu được thay đổi bởi Kru, thể tích nước tiêu nên được đo hàng tháng.
Phương pháp đo Kru gồm lấy nước tiêu để đo độ thanh thải của ure và/hoặc creatinin và sử dụng marker lọc ngoại sinh như iothlamate để đo độ thanh thỉ. Như đã chú ý ở trên, ure là đặc biệt hữu ích để đo độ thanh thải lọc máu và thận và có thể được phối hợp sử dụng các công thức hiện nay với nồng độ trung bình của ure trong thua thập nước tiểu ước tính từ mẫu máu trước và sau lọc hoặc mô hình toán học của hình thái nồng độ ure (xem mục 2 trong Phụ lục). Để phối hợp Kt/V ngắt quãng với Kru, các phương pháp đã được phát triển để tính toán cho hiệu quả cao hơn của Kru liên tục Kru so sánh cới độ thanh thải quả lọc ngắt quãng (xem mục 4 trong Phụ lục, và cả hai phụ lục7(ppS75-S77) và các khuyến cáo thực hành cho tuyên bố hướng dẫn 2 trong hướng dẫn của KDOQI trước đây).7
Lịch HD không phải ba lần hàng tuần (Hướng dẫn 3.3)
stdKt/V là tỷ lệ sản sinh ure hàng tuần được cho là một nhân tố bằng nồng độ ure máu trước lọc trung bình của một tuần.144,145 Bằng định nghĩa, nó bao gồm các yếu tố góp phần của siêu lọc trong quá trình lọc máu và Kru.146 stdKt/V bắt nguồn từ nỗ lực để tính toán cho cải thiện hiệu quả củ điều trị lọc máu liên tục và nhiều lần hơn so sánh với HD ngắn quãng, và dựa trên so sánh nòng độ chấ tan trung bình đạt được trong HD và PD. stdKt/V được chú ý là độ thanh thải cân bằng liên tục mà cho phsp so sánh liên tục với lọc máu ngắt quãng và dựa trên cân bằng của các kết quả được lọc với PD liên tục và người được điều trị HD ba lần hàng tuần.145,144 Mô tả chi tiết hơn của stdKt/V có thể tìm thấy trong hướng dẫn KDOQI trước đây ở các Hướng dẫn thực hành lâm sàng 2 và 4.7 stdKt/V có thể được tính từ spKt/V sử dụng các công thức toán hoạc mà có điều chỉnh theo siêu lọc và Kru (mục 3 trong Phụ lục).146
Khi cả stdKt/V được bình thường hóa bởi V, thê tích phân bố ure (nước) của bệnh nhân, cả hai được ước tính thấp ở bệnh nhân có kích thước nhỏ và ở phụ nữ. Nỗ lực đã được tạo ra để loại bỏ lỗi này bằng tích hợp với diện tích da (BSA) dưới dạng mẫu số và được chỉ ra trong mục 4 của Phụ lục.147 BSA cho V trong mẫu số giảm lỗi khi bệnh nhân mất cân hoặc tăng phù, không những ảnh hướng đến lọc máu mà làm thay đổi đáng kể Kt/V.
Hạn chế của Các hướng dẫn
Các nghiên cứu của các yêu cầu trong cộng đồng đã chỉ ra các kết quả lâm sàng được tối ưu khi bệnh nhân đã được điều trị với liều lọc máu phân phối đã khuyến cáo trong các hướng dẫn đó.127,129 Khi đo liều bằng độ thanh thải các chất hòa tan nhỏ được đưa ra rằng công nhận thiếu đi các hiểu biết về độc tính cụ thể dẫn đến mất chức năng thận, có thể và có lẽ rằng một bệnh nhân không thường xuyên sinh độc tố ở tốc độ cũng như mức độ trung bình và do đó cần nhiều lần lọc máu hơn như đã được khuyến cáo bởi các hướng dẫn. Các nhà lâm sàng nên cảnh báo với các triệu chứng và dấu hiệu của suy thận mà có thể chỉ ra sự cần thiết tăng lọc máu hoặc các phương thức lọc máu khác. Các chỉ định có thể cho lọc máu nhiều lần hơn mức độ đã khuyến cáo được liệt kê ở Hướng dẫn 4.
Sau khi ảnh hưởng đe dọa chức năng sống cấp của tăng ure máu đã được kiểm soát bởi HD tiêu chuẩn, bệnh nhân thường mất đi các triệu chứng và các rối loạn mà đã được cộng gộp lại với nhau thành “hội chứng dư thừa”.130,148 Tác dụng phối hợp của trạng thái rối loạn này có thể tăng tỷ lệ tử vong tương đối cao đã được quan sát ở cộng đồng lọc máu. Nhiều trường hợp, để giảm nhẹ hội chứng cần các điều trị bổ sung, hiện nhiều nơi vân chưa sẵn có cho các nhà lâm sàng. Các khía cạnh đã biết gồm thiếu máu, cường cận giáp, ngứa, trầm cảm, thiếu protein năng lượng, toàn bộ trong số đó có thể đáp ứng với điều trị mà độc lập với lọc máu. Các nguyên nhân của bệnh thận của bệnh nhân (như đái tháo đường hoặc lupus ban đỏ hệ thống) có thể liên tục tác động và góp phần vào hội chứng. Các nguyên nhân khác của hội chứng đã được đưa ra, gồm ảnh hưởng của protein cabmyl hóa, độc tố gắn kết với protein, sản phẩm cuối của glycosylate tiến triển (AGE), các yếu tố trung gian gây viêm, và các chất tan khác vẫn chưa được loại bỏ bởi lọc máu tiêu chuẩn.
Nghiên cứu lại khuyến cáo
Các nghiên cứu lại tương lai nên trực tiếp đê hiểu biết tốt hơn về hội chứng còn lại với tâm điểm trên điều trị và cảu thiện tỷ lệ sống trong khi không làm mất đi dấu ấn của loại bỏ chất tan nhỏ, mà phải được chú ý là một khía cạnh quan trọng nhất của HD.
PHỤ LỤC CỦA HƯỚNG DẪN 3
1. Phương pháp đo spKt/V từ logarit tự nhiên của tỷ lệ BUN trước và sau lọc
Một công thức tuyến tính đã được phát triển và đã được chỉ ra là ước tính spKt/V từ logarit tự nhiên đem đến các kết qủa đáng tin cậy cho khi ứng dụng trong HD 3 lần mỗi tuần
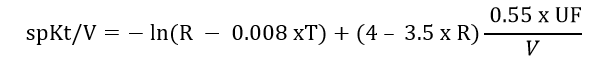
Trong đó: R là tỷ lệ BUN trước lọc và BUN sau lọc; V là thể tích nước trong có thể và UF là lượng siêu lọc (cân trước lọc trừ cân sau lọc) ở cùng đơn vị với V; và T là thời gian điều trị tính bằng giờ.
Tuy nhiên, với lịch điều trị khác gồm từ 2 đến 7 lần mỗi tuần, các kết quả sẽ khác với chỉ số Kt/V đánh giá bằng công thức mô hình động học ure. Sai số là lớn do sự khác biệt do ảnh hưởng của sản sinh ure giữa các lần lọc máu. Một thay đổi gần đây đã được thiết lập tính toán cho biến này và loại trừ các sai sót đó là:
![]()
Công thức này khác với công thức trên bởi thay thế 0.008 bằng chỉ số GFAC (yếu tố G). GFAC là thuật ngữ mà giảm R để ước tính chỉ số trong sự vắng mặt của sản sinh ure và trong khoảng từ 0.0045 đến 0.0175, phụ thuộc vào tần xuất lọc máu, nhưng hàu hết là phụ thuộc vào khoảng cách với lần lọc máu trước (PIDI). Chỉ số này có thể lấy được từ một bảng đã được công bố và có thể ước tính thô bằng 0.175 chia cho PIDI (ngày).
2. Phương pháp ước tính Kru từ mẫu máu ở thời điểm bắt đầu và kết thúc thu thập nước tiểu
Nồng độ BUN thay đổi nhiều trong HD và giữa hai lần lọc máu, vì vậy BUN trung bình trong quá trình lấy nước tiểu phải được xác định để tính độ thanh thải. Mô hình chính thức cho phép ước tính chính xác hơn mà không cần lấy xét nghiệm máu nhiều lần, nhưng hiện đang không có chương trình tích hợp vấn đề này. BUN trung bình có thể ước tính từ BUN máu ở thời điểm bắt đầu và kết thúc lấy nước tiểu. Thời gian thu thập nước tiểu nên mở rộng từ cuối buổi HD đến khi bắt đầu buổi lọc sau. Với một sự thích hợp, BUN trung bình trước và sau HD được đo có thể được sử dụng để tính Kru. Kru có thể phối hợp với độ thanh thải quả loci hoặc bằng thêm trực tiếp vào stdKt/V như được chỉ ở dưới (mục 3 của Phụ lục) hoặc bằng sử dụng chính chỉ số của nó để có hiệu quả cao hơn của độ thanh thải liên tục, sau đó nó được thêm vào spKt/V như đã chỉ ra trong phụ lục của hướng dẫn KDOQI trước đây.
3. Phương pháp ước tính stdKt/V từ spKt/V
stdKt/V được phát sinh bởi Gotch145 như một phương pháp cho đánh giá độ thanh thải quả lọc ngắt quãng thứ cấp để cân bằng với độ thanh thải liên tục bằng việc xác định lại độ thanh thải khi tốc độ sản sinh ure (G) được chi bởi BUN trước lọc trung bình (avCpre). Việc tính toán dựa trên mô hình thể tích hỗn hợp của động học ure trong toàn bộ cả tuần. Phương pháp gốc đõ được Leypoldt đơn giản hóa150 và sau đó đã hoàn chỉnh bởi Daugirdas và cộng sự146, ông đã đưa tốc độ siêu lọc (UF) và Kru vào công thức. Như được định nghĩa ban đầu bởi Gotch, stdKt/V gồm ảnh hưởng của UF và Kru. Tuy nhiên, khi đo sử dụng chỉ số G, eKt/V, và avCpre, sự đóng góp của Kru giả định rằng Kru chỉ sử dụng avCpre thay thế của BUN trung bình trong mẫu số. Để điều chỉnh cho sai sót này khi đưa Kru vào, các chỉ số mô hình cho G và V phải được sử dụng để tính stdKt/V mà không có Kru, mà có thể sau đó thêm Kru x 10.808/V146
Các công thức sau đây cho phép ước tính tương đối đúng của stdKt/V thực từ spKt/V với độ chính xác được nâng lên bằng UF và Kru.145,146,150
eKt/V = spKt/V (t/t+30))151
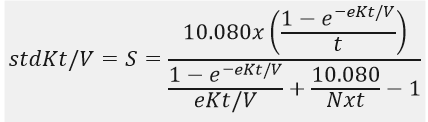
(Mô hình thể tích hỗn hợp, không Kru)

(mô hình thể tích biến đổi với Kru)
Trong đó: S chính là stdKt/V từ mô hình thể tích hỗn hợp (công thức thứ hai); N là số buổi lọc mỗi tuần; UF là thể tích siêu lọc hàng tuần (mL); V là thể tích phân bổ ure tính bằng mL; Kru là độ thanh thải thận tự nhiên còn lại của ure tính bằng mL/phút; 10.080 là số phút trong một tuần.
Khi không có Kru, công thức sau cùng ở trên sẽ đem lại chỉ số stdKt/V cao hơn ~7% trung bình của công thức trước.
Để đề phòng bệnh nhân chạy thận dưới mức, sự có mặt của Kru nên được thêm vào chỉ nếu đo được làm trong thời gian 3 tháng trước ngày đưa vào mô hình tính toán.
4. Phương thức tính SAstdKt/V
Thể tích phân bổ ure (V) trong mẫu số của diễn giải độ thanh thải ure (Kt/V) là có vấn đề. V thông thường có trong sự diễn giải của độ thanh thải khi được tính bằng xét nghiệm ure đơn độc trước và sau lọc máu, và khi đo thể tích toàn bộ cơ thể có liên quan chặt chẽ đến khối cơ thể, mà thường được sử dụng để tính toán liều thuốc. Tuy nhiên, mẫu số thường được sử dụng cho xác định các chức năng sinh lý của chức năng thận tự nhiên là BSA. Một phân tích thứ phát của dữ liệu nghiên cứu HEMO, cho thấy cải thiện kết quả ở nữ giới nhưng không có ở nam giới điều trị với liều HD cao, tăng mối quan tâm về sự không phụ hợp có thể sử dụng V khi dùng làm mẫu số ở nữ giới và bệnh nhân nhỏ (Xem Hình 3).147,152. Các nỗ lực để loại bỏ rào cản này ở cả phụ nữ và bệnh nhân nhỏ đã đưa ra sự diễn giả stdKt/V với BSA trong mẫu số mà vẫn giữ lại các chỉ số mục tiêu hiện nay146,153,154.
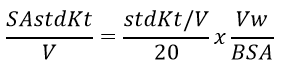
SAstdKt/V là Kt/V tiêu chuẩn hóa với diện tích da (phần/tuần); Vw là thể tích phân bổ ure của bệnh nhân xác định bằng công thức Watson (L)155; BSA là diện tích cơ thể dựa trên chiều cao và cân nặng (m2)156; và 20 là yếu tố bình thường hóa (trung bình V/BSA, L/m2 cộng đồng). Yếu tố bình thường hóa có thể khác 20 khi sử dụng các công thức khác công thức Watson và cs155 và công thức DuBois và DuBois156 để ước tính V và BSA, tương ứng, ví dụ như ở trẻ em.
5. Phương pháp và công thức đo độ dẫn điện dịch lọc
D = [Qd + Qf][1-(Co1 – Co2)/Ci1 – Ci2)]157
Co và Ci là độ dẫn điện dịch ra và vào (mSe/cm); D là thanh thải lọc (ml/phút); Qd là lưu lượng dịch lọc; và Qf là lưu lượng siêu lọc.
Thanh thải lọc ở đây được sử dụng bởi độ dẫn điện dòng và khác 0. Trong thực hành, thanh thải lọc độ dẫn điện là đo độ thanh thải chất tan nhỏ bởi chúng chịu trách nhiệm cho độ dẫn điện dịch lọc là nhỏ (hầu hết là Na và anion) và được lọc dễ dàng. Thanh thải lọc độ dẫn điện có tương quan cao với thanh thải ure.135,157
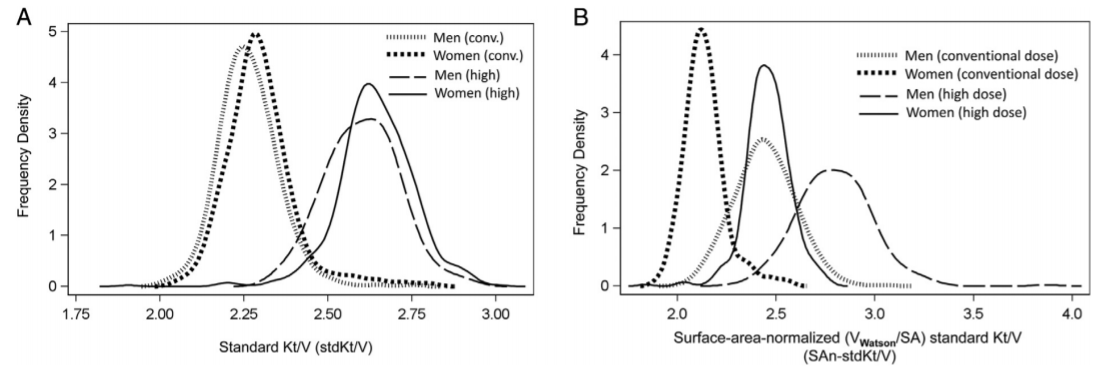
Hình 3: Liều lọc máu phân phối trong Nghiên cứu HEMO. (A) Sự phân chia rõ ràng của liều lọc máu biểu hiện Kt/V đạt được cho toàn bộ bệnh nhân trong nghiên cứu HEMO. (B) Khi bình thường hóa với BSA, phụ nữ ngẫu nhiên có liều cao hơn so sánh với nam giới lọc máu thông thường129. Reproduced with permission of the American Society of Nephrology from Daugirdas et al.147
BSCKI Nguyễn Thanh Hùng
dịch từ KDOQI CLINICAL PRACTICE GUIDELINE FOR HEMODIALYSIS ADEQUACY: 2015 UPDATE – https://www.kidney.org/professionals/guidelines/hemodialysis2015