Dịch: BSCKI Nguyễn Thanh Hùng, Phó TTK Hội Lọc máu Việt Nam
CHƯƠNG 5: CHẨN ĐOÁN VÀ QUẢN LÝ BỆNH THẬN LIÊN QUAN VỚI HCV
Ngoài bệnh gan mạn, nhiễm HCV có thể dẫn đến nhiều biểu hiện ngoài gan, bao gồm bệnh thận và cryoglobulin máu hỗn hợp. Mặc dù nhiễm HCV mạn có thể gây ra các tổn thương ống kẽ thận, GN liên quan đến HCV là loại bệnh thận thường gặp nhất, với MPGN trở thành tổn thương phổ biến nhất.277,278 Tuy nhiên, tỷ lệ phát sinh của GN liên quan HCV là thấp, như đã được xác nhận gần đây bởi một nghiên cứu phạm vi lớn. Moorman và cộng sự297 thấy tần xuất của hội chứng thận hư là 0.3% ở đoàn hệ lớn bệnh nhân nhiễm HCV RNA, tần xuất cryoglobulin máu là 0.9%. Các kết quả tương tự đã được cung cấp bởi Nationwide Inpatient Sample of the Healthcare Cost and Utilization Project, mà đã được kiểm tra các bệnh đồng mắc ở bệnh nhân chẩn đoán nhiễm HCV ở bệnh nhân nội trú tại Hoa Kỳ từ năm 2004 đến 2011. Tỷ lệ Hội chứng thận hư hoặc MPGN nằm trong khoảng 0.47% và 0.36%.280 Theo một nghiên cứu đoàn hệ hồi cứu ở những bệnh nhân Cựu Chiến binh với xét nghiệm HCV RNA dương tính, những người đã nhận được thời gian điều trị DAA lần đầu từ năm 2012 đến 2016 (n=45.260), tỷ lệ lưu hành ban đầu của GN (Chẩn đoán theo Mã Phân loại Bệnh Quốc tế [ICD]-9/10) là xung quanh 2.6%.281
Gánh nặng ngoài gan của nhiễm HCV được đánh giá bởi El-Serag và cộng sự, người đã tiến hành nghiên cứu đối chứng ca bệnh nhập viện nội trú ở cựa chiến binh nam giới Hoa Kỳ từ năm 1992 đến năm 1999. Họ đã xác nhận 34.204 bệnh nhân nhiễm HCV (nhóm bệnh) và 136.816 bệnh nhân không nhiễm HCV (nhóm chứng) lựa chọn ngẫu nhiên.282 Tỷ lệ MPGN lớn hơn (0.36% vs. 0.05%, P < 0.0001) nhưng bệnh thận mạn thì không (0.33% vs. 0.19%, P=0.86) đã được tìm thấy ở bệnh nhân nhiễm HCV. GN liên quan HCV xảy ra thường liên quan với cryoglobuline hỗn hợp, một viêm mạch máu hệ thống, đặc trưng bởi các mạch máu kích thước nhỏ, ít gặp hơn với các mạch máu kích thước trung bình.277,278,283-285 Cryoglobulin máu xuất hiện từ 60% đến 75% toàn bộ các ca bệnh cryoglobulin máu và quan sát được ở bệnh nhân có bệnh mô liên kết, nhiễm trùng mạn hoặc rối loạn hình thái tế bào lympho, toàn bộ chúng được phân loại vào nhóm với thuật ngữ “cryoglobuline máu hỗn hợp thứ phát”. HCV có liên quan đến 80 – 90% nguyên nhân với các ca bệnh cryoglobuline máu trước đây cho là “vô căn”.283,284 Nhìn chung, HCV có liên quan với cryoglobulin máu hỗn hợp tuýp II (cryoglobulin chứa IgG đa dòng và IgM đơn dòng với hoạt tính yếu tố dạng thấp), dù nó ít liên quan với cryoglobulin máu hỗn hợp tuýp III (cryoglobulin chứa IgG đa dòng và IgM đa dòng).
| 5.1 |
Bệnh nhân nhiễm HCV với sự xuất hiện của viêm cầu thận tăng sinh phức hợp miễn dịch có thể được quản lý mà không cần sinh thiết thận xác nhận. Tuy nhiên, sinh thiết thận có thể được chỉ định ở một số trường hợp lâm sàng nhất định (Hình 4) (Không phân độ). |
||
| 5.2 |
Chúng tôi khuyến cáo rằng bệnh nhân viêm cầu thận liên quan đến HCV nhận được điều trị kháng virus (1A) |
||
| 5.2.1. |
Chúng tôi khuyến cáo rằng bệnh nhân có viêm cầu thận liên quan đến HCV, chức năng thận ổn định, và không có hội chứng thận hư được điều trị DAA trước khi điều trị khác (1C). |
||
| 5.2.2. |
Chúng tôi khuyến cáo rằng bệnh nhân bùng phát cryoglobulin máu hoặc viêm cầu thận tiến triển nhanh được điều trị DAA và thuốc ức chế miễn dịch có hoặc không có thay huyết tương (1C). |
||
| 5.2.2.1. |
Quyết định liệu sử dụng thuốc ức chế miễn dịch ở bệnh nhân hội chứng thận hư hay không nên được cá nhân hóa (Không phân độ). |
||
| 5.2.3 |
Chúng tôi khuyến cáo điều trị ức chế miễn dịch ở bệnh nhân viêm cầu thận liên qua HCV hoạt động trên mô bệnh học những người mà không đáp ứng với điều trị kháng virus, đặc biệt người có bệnh thận cryoglobuline máu (1B). |
||
| 5.2.3.1. |
Chúng tôi khuyến cáo rituximab là lựa chọn điều trị ức chế miễn dịch đầu tay (1C). |
||
GIẢI THÍCH
| 5.2 |
Bệnh nhân nhiễm HCV với sự xuất hiện của viêm cầu thận tăng sinh phức hợp miễn dịch có thể được quản lý mà không cần sinh thiết thận xác nhận. Tuy nhiên, sinh thiết thận có thể được chỉ định ở một số trường hợp lâm sàng nhất định (Hình 4) (Không phân độ). |
Biểu hiện lâm sàng của bệnh cầu thận ở bệnh nhân nhiễm HCV bao gồm xuất hiện của protein niệu và/hoặc hồng cầu niệu vi thể, có hoặc không có giảm GFR. Vẫn chưa rõ ràng tại sao một phần nhỏ bệnh nhân nhiễm HCV xuất hiện các bất thường tại thận, mặc dù đa hình thái nhiều kiểu gen đã được đề nghị như là yếu tố nguy cơ cho sự hình thành cryoglobulin máu.286-288 Bệnh cầu thận liên quan với nhiễm HCV đã được mô tả trong sự có mặt hoặc không có mặt của bệnh gan rõ rệt.289,290
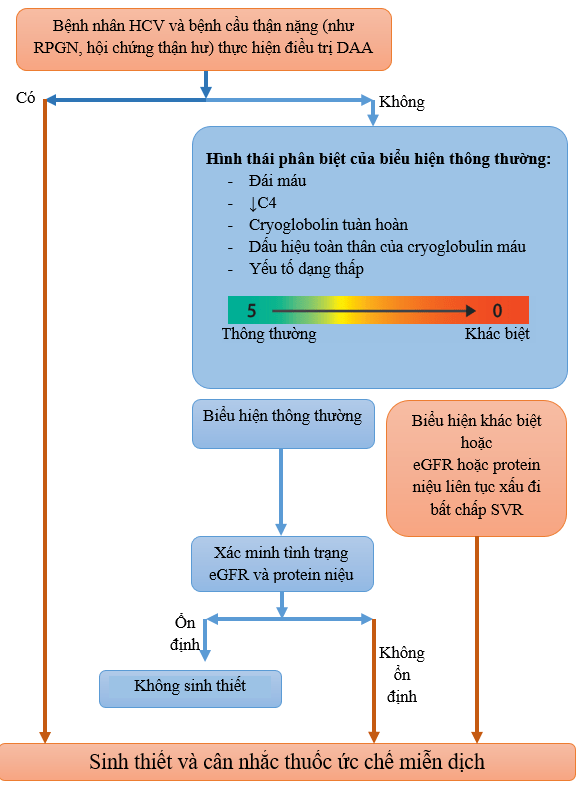
Hình 4|Chỉ định sinh thiết thận ở bệnh nhân có viêm gan virus C và bệnh cầu thận nặng. Sơ đồ trên giả định rằng bệnh nhân HCV và HCV và bệnh thận mạn (CKD) nhận được thuốc kháng virus hoạt tính trực tiếp. Dấu hiệu toàn thận của cryoglobulin máu gồm các tổn thương da như ban xuất huyết, đau khớp và yếu mệt. eGFR, Mức lọc cầu thận; RPGN, bệnh cầu thận tiến triển nhanh; SVR, đáp ứng virus bền vững.
Chỉ định sinh thiết thận ở bệnh nhân nhiễm HCV và dấu hiệu bệnh cầu thận không có khác biệt rõ ràng với các chỉ định sinh thiết thận thông thường ở bệnh cầu thận khác.291 Sinh thiết thận vẫn còn có giá trị để đánh giá hình ảnh mô bệnh học của bệnh và có lẽ các tổn thương quan sát được cho biết nguyên nhân liên quan đến nhiễm HCV. Bệnh cầu thận khác (như bệnh thận đái tháo đường) không thường xuyên được báo cáo ở bệnh nhân nhiễm HCV.292 Một phần kết quả này từ thực tế rằng tỷ lệ phát sinh đái tháo đường đã được biết là lớn hơn ở bệnh nhân nhiễm HCV so với cộng đồng chung.293,294 Ngoài ra, mô bệnh học sẽ cung cấp đánh giá sự lan tỏa của tổn thương hoạt động mà có thể định hướng để điều trị ức chế miễn dịch so với tổn thương mạn dường như không đáp ứng với ức chế miễn dịch. Do đó, một số bệnh nhân có thể tránh được thuốc ức chế miễn dịch khi có sự xuất hiện của tổn thương mạn tính nặng miễn là không có chỉ định ngoài thận với thuốc ức chế miễn dịch.291
Hầu hết bệnh nhân HCV mạn (có hoặc không có GN) nên được điều trị với DAA, sinh thiết thận có thể không thay đổi quản lý ở phần lớn bệnh nhân nhiễm HCV và tổn thương thận. Hầu hết bệnh nhân GN HCV có thể được quản lý mà không sinh thiết thận nếu có một đề nghị mạnh của GN hoạt động dựa trên sự xuất hiện triệu chứng lâm sàng thông thường (đái máu, protein niệu, giảm GFR chậm). Trong một nghiên cứu gần đây bởi Perez de Jose và cộng sự,295 hơn 50% bệnh nhân cryoglobuline máu hỗn hợp HCV với bệnh thận được điều trị DAA dựa trên biểu hiện lâm sàng, không có sinh thiết thận. Điều trị DAA không nên chậm chễ hoặc trì hoãn trong khi đợi kết quả sinh thiết thận. Đây là một thực tế đặc biệt ở bệnh nhân bệnh gan mạn mà sẽ có nguy cơ chảy máu sau sinh thiết cao (do bệnh chảy máu, bệnh đông máu, giãn tĩnh mạch sau phúc mạc, …). Tuy nhiên, nếu dấu hiệu lâm sàng của bệnh thận (đái máu, giảm GFR, albumin niệu) không cải thiện hoặc ít ổn định bất chấp đã đạt được SVR, hoặc nếu bằng chứng bệnh thận tiến triển nhanh, sinh thiết thận có thể được cảnh báo để xác nhận chẩn đoán trước khi bắt đầu điều trị ức chế miễn dịch.
Sinh thiết thận do đó không phải là điều kiện để bắt đầu điều trị DAA cho điều trị GN liên quan HCV; tuy nhiên, sinh thiết thận nên được tiến hành nếu lập kết hoạch điều trị ức chế miễn dịch hoặc một chẩn đoán phân biệt với nghi ngờ bệnh GN liên quan đến HCV khác (Hình 4). Với chiến lược đó, nguy cơ nhỏ nhưng không đáng kể của các biến chứng từ sinh thiết thận có thể tránh cho phần lớn bệnh nhân. Tổng hợp hệ thống296,297 đã tìm thấy rằng sau sinh thiết thận, nguy cơ chảy máu cần truyền máu khoảng 1% đến 1.5%; cần can thiệp để ngừng chảy máu xung quanh 0.3%; nguy cơ tử vong xấp xỉ 0.06%.
Loại GN liên quan đến HCV phổ biến nhất trên sinh thiết thận là MPGN trung gian phức hợp miễn dịch, thường phản ánh sự xuất hiện của cryoglobulin máu tuýp II. Hình thái mô bệnh học khác biệt của cryoglobulin máu, đặc biệt ở bệnh nhân giảm chức năng thận tiến triển, bao gồm lắng đọng trong cầu thận, hay thấy ở lớp dưới nội mô. Lắng đọng cryoglobulin có thể thỉnh thoảng làm tắc mao mạch (nhìn thấy huyết khối trong nòng mạch với bạch cầu ái toan trên kính hiểm vi quang học). Cầu thận có thể cho thấy tăng sinh tế bào như là hậu quả của thâm nhiễm mao mạch cầu thận bởi bạch cầu đơn nhân và đa nhân. Cầu thận thường cho thấy cấu trúc dạng búi với phối hợp của tăng cấu trúc và tế bào gian mạch, sưng phồng tế bào nội mô, tách màng đáy trong và tích lũy vật liệu ái toan biểu hiện của phức hợp miễn dịch hoặc cryoglobuline. Màng đáy cầu thận thường có hình viền đôi bởi xâm nhiễm của tế bào mono giữa màng đáy và nội mô. Trên kính hiểm vi điện tử, lắng đọng dưới nội mô lớn. Viêm mạch máu ở động mạch thận nhỏ xuất hiện ở 30% trường hợp.298 Hình thái mô bệnh học MPGN lan tỏa hoặc tiểu thùy là liên quan đến sự xuất hiện của hội chứng thận hư và/hoặc viêm thận, trong khi tăng sinh gian mạch và mở rộng cấu trức xuất hiện trong các trường hợp tác động lên chức năng thận và protein niệu và/hoặc đái máu vi thể.298
Những trường hợp MPGN liên quan đến HCV mà không có cryoglobuline máu không thường xuyên được báo cáo.278 Ở những bệnh nhân đó, hình ảnh lâm sàng, hình thái mô bệnh học, và dữ liệu xét nghiệm là không phân biệt được với MPGN trung gian phức hợp miễn dịch “cổ điển”. Cả phức hợp miễn dịch dưới nội mô và gian mạch có thể được xác nhận trên kính hiểm vi điện tử, thông thường mà không có phân biệt dưới cấu trúc. Ở cả hai dạng GN liên quan đến HCV, miễn dịch huỳnh quang cho thấy lắng đọng IgM, IgG, và C3 ở trung gian và thành mao mạch.
Bệnh thận màng thụ thể phospholipase A2 (PLA2R) âm tính được quan sát thấy trong mối liên quan với nhiễm HCV mạn.263 Mối liên quan này là thực hay không vẫn chưa rõ ràng. Bệnh cầu thận khác thỉnh thoảng được báo cáo ở nhiễm HCV mạn là GN tăng sinh cấp, xơ hóa cầu thận khu trú từng vùng,299 bệnh thận IgA,300 GN xơ hóa, và bệnh thận immunotactoid.302 Tuy nhiên, mối liên kết bệnh lý đó với HCV vẫn chưa biết một cách rõ ràng so với bệnh thận màng.
Bệnh sinh của bệnh cầu thận liên quan đến HCV gồm tổn thương trung gian miễn dịch (bao gồm ảnh hưởng từ cryoglobulin máu) cũng như tác động trực tiếp của virus lên mô thận. HCV được cho là gắn kết và xâm nhập vào tế bào nhu mô thận qua thụ thể CD81 và SR-B1.303,304 HCV RNA đã được tìm thấy trong tế bào gian mạch, tế bào biểu mô ống thận, và tế bào nội mô của cầu thận và mao mạch ống thận. Sự lắng đọng của phức hợp miễn dịch chứa protein của HCV ở màng đáy cầu thận đã được cho là nằm trong cơ chế bệnh sinh của bệnh thận màng liên quan đến HCV.303,304 Lắng đọng protein dạng hạt liên quan đến HCV ở gian mạch đã được quan sát ở bệnh nhân MPGN liên quan HCV; chúng có lẽ liên quan đến mức độ protein niệu cao hơn.305 Kháng nguyên virus đã được tìm thấy bởi mô hóa miễn dịch,306 lai tạo tại chỗ,306 và chụp vi phẫu lazer.307
| 5.2 |
Chúng tôi khuyến cáo rằng bệnh nhân viêm cầu thận liên quan đến HCV được điều trị kháng virus (1A) |
|
| 5.2.1. |
Chúng tôi khuyến cáo rằng bệnh nhân có viêm cầu thận liên quan đến HCV, chức năng thận ổn định, và không có hội chứng thận hư được điều trị DAA trước khi điều trị khác (1C). |
|
Đang thiếu các RCT để giúp thiết lập các khuyến cáo dựa trên bằng chứng cho điều trị các tổn thương cầu thận liên quan đến nhiễm HCV. Cho đến khi thông tin này sẵn có, điều trị GN liên quan đến HCV nên được thực hiện theo mức độ nặng của protein niệu và suy thận. Tuy nhiên, với điều trị DAA hiện nay rất sẵn có, toàn bộ bệnh nhân nhiễm HCV là ứng viên cho điều trị kháng virus này.
Sự hình thành bệnh thận ở bệnh nhân cryoglobulin máu hỗn hợp có vai trò đặc biệt quan trọng bởi ảnh hưởng đến thận dự báo một tiên lượng kém.308-310 Tổng hợp vai trò của HCV trong cơ chế bệnh sinh của GN cryoglobulin máu, điều trị kháng virus đã được sử dụng để thải sạch nhiễm HCV và cải thiện tổn thương thận. Bằng chứng về hướng tác động của điều trị kháng virus của GN liên quan đến HCV, cho đến gần đây, là rất hạn chế và hầu hết là các báo cáo không hoàn toàn chính xác và các nghiên cứu quan sát cỡ mẫu nhỏ.
Với những gì mang lại của DAA, các phác đồ dựa trên IFN hiện nay đã trở lên lỗi thời. Các nghiên cứu kháng virrus trước đây311-313 phần nào đó cung cấp cái nhìn có giá trị vào vai trò căn nguyên của HCV trong cơ chế bệnh sinh của GN, cũng như thông tin về lợi ích của điều trị kháng virus trên thận.
Một tổng hợp hệ thống cũ của các nghiên cứu so sánh IFN so với các phác đồ ức chế miễn dịch cho GN do HCV đề nghị một số lợi ích trong giảm protein niệu, nhưng với ước tính mức độ chính xác không cao: odds ratio (OR) 1.92; 95% CI: 0.39–9.57.314 Chú ý, ở toàn bộ bệnh nhân giảm protein niệu, thanh thải HCV RNA đã quan sát được ở cuối liệu trình kháng virus.314
Một tổng hợp hệ thống sau này75 kết luận rằng liệu trình IFN-α giảm protein niệu ở bệnh nhân nhiễm HCV có CKD. Ở cuối của liệu trình kháng virus, ước tính tổng của giảm trung bình protein niệu là 2.71 g/24 h (95% CI: 1.38–4.04). Giảm protein niệu sau điều trị kháng virus phản ánh thanh thải HCV RNA. Mặc dù, creatinin huyết thanh đã không cải thiện có ý nghĩa sau điều trị IFN-α, nhưng sự ổn định của creatinin huyết thanh đạt được.
Với sự thuyên giả của đái máu, protein niệu, và cải thiện GFR ở bệnh nhân GN liên quan đến HCV sau khi thanh thải HCV RNA bằng DAA,266-275 điều trị kháng virus với phác đồ DAA nên được cân nhắc là lựa chọn điều trị đầu tay ở bệnh nhân không có hội chứng thận hư và chức năng thận tương đối ổn định (Bảng Bổ sung S24 – S26). Ngoài ra, điều trị tiêu chuẩn đối với CKD protein niệu nên được thực hiện. Điều trị này bao gồm kiểm soát huyết áp tối ưu, thường bằng nhiều loại thuốc, trong đó có lợi tiểu.315 Hơn nữa, ức chế men chuyển angiotensin hoặc chẹn thụ thể angiotensin nên được sử dụng để điều trị protein niệu.53
Các kết quả đáng khích lệ đã thu được từ các phác đồ DAA không có IFN đối với GN liên quan HCV. Tổng hợp hệ thống của chúng tôi thấy SVR12 rất cao ở bệnh nhân cryoglobulin máu liên quan HCV (Bảng Bổ sung S24 và S26). Qua 5 nghiên cứu với 1294 bệnh nhân, trong đó có 479 bệnh nhân GN, SVR12 sau rất nhiều điều trị DAA khác nhau là 99.0% (95% CI: 97.7%–99.8%).
Ngoài ra, GN HCV mới mắc,316,317 GN HCV bền bỉ,316,318 hoặc cryoglobulin huyết thanh bền bỉ319 sau điều trị DAA thành công vẫn thỉnh thoảng bắt gặp. Người ta đề nghị rằng ở nhóm bệnh nhân này, GN liên quan HCV có thể bền bỉ bất chấp đạt được SVR12, dường như do dòng tế bào B tồn dư tạo ra yếu tố dạng thấp. GN HCV mới mắc sau rituximab đã được chú ý, và nó được đóng góp do bùng nổ HCV sau dùng rituximab.
Trong 45.260 bệnh nhân HCV RNA dương tính được điều trị với nhiều phác đồ DAA khác nhau (có hoặc không có RBV) (thời gian theo dõi trung bình là 2.01 năm) ở Ban Cựu Chiến binh Mỹ, 41,711 (92.2%) đạt được SVR. Mô hình nguy cơ đầy đủ cho thấy rằng tỷ lệ phát sinh GN sau SVR là giảm đáng kể, HR điều chỉnh là 0.61 (95% CI: 0.41–0.90; P ¼ 0.0126).281
Các nghiên cứu đó đề nghị rằng các phác đồ không IFN (và thông thường, các phác đồ không có RBV) với DAA có đáp ứng virus học và lâm sàng tuyệt vời trong những điều kiện điều trị khó khăn như cryoglobulin hỗn hợp liên quan đến HCV với tổn thương thận hoặc GN liên quan HCV không cryoglobulin máu. Tuy nhiên, các nghiên cứu lớn hơn và đối chứng được chào mời để xác nhận các kết quả đó.
Tổng hợp hệ thống của chúng tôi hỗ trợ sự chú ý rằng DAA có tác động có lợi lên bệnh nhân và tỷ lệ sống thận (Bảng Bổ sung S24 và S26). Trong một nghiên cứu đa trung tâm từ Tây Ban Nha,295, 139 bệnh nhân cryoglobulin máu hỗn hợp HCV (65 bệnh nhân GN HCV trên sinh thiết) được theo dõi với thời gian trung vị là 138 tháng. Ở 100 bệnh nhân được điều trị với DAA không xác định, 4% tử vong và 6% có creatinin tăng gấp đôi hoặc suy thận. Ngược lại, ở 15 bệnh nhân không được điều trị, 2/3 tử vong và 20% tăng gấp đôi creatinin hoặc suy thận. HR cho tỷ lệ tử vong sau điều trị DAA là 0.12 (95% CI: 0.04–0.40), HR cho tăng gấp đôi creatinin hoặc suy thận là 0.10 (95% CI: 0.04–0.33). Qua 4 nghiên cứu, với 1172 bệnh nhân viêm mạch máu cryoglobulin máu, trong đó 506 có GN, tỷ lệ tử vong sau điều trị 1 năm là 2.4% (95% CI: 1.6%–3.4%), và trong 2 nghiên cứu (n=156), tăng gấp đôi creatinin hoặc suy thận xảy ra ở 3.8% (95% CI: 1.7%–8.3%) bệnh nhân.
Bất chấp hiệu quả ấn tượng này, điều trị kháng virus của GN liên quan đến HCV vẫn có một số hạn chế. Lợi ích lâm sàng ở bệnh nhân đạt được SVR có thể thỉnh thoảng là tạm thời, và sự phân li giữa đáp ứng virus học và trên thận có thể xảy ra.287,320-322 Các nghiên cứu thời gian dài đó (1 đến 2 năm) báo cáo tỷ lệ cao của cải thiện rõ ràng rất nhiều biểu hiện liên quan đến cryoglobulin máu sau khi SVR với DAA, nhưng xác nhận rằng tái phát viêm mạch máu có thể xảy ra bất chấp đạt được SVR.323-325.
| 5.2.2. |
Chúng tôi khuyến cáo rằng bệnh nhân bùng phát cryoglobulin máu hoặc viêm cầu thận tiến triển nhanh được điều trị DAA và thuốc ức chế miễn dịch có hoặc không có thay huyết tương (1C). |
|
| 5.2.2.1. |
Quyết định liệu sử dụng thuốc ức chế miễn dịch ở bệnh nhân hội chứng thận hư hay không nên được cá nhân hóa (Không phân độ). |
|
Các thuốc ức chế miễn dịch được đưa thêm vào bệnh nhân có biến chứng nặng, đe dọa tính mạng của cryoglobulin máu hỗn hợp, như MPGN, bệnh thận nặng, hoặc bệnh da lan tỏa như ung thư hoặc ban xuất huyết hoạt tử. Rituximab, một kháng thể đơn dòng chimeric, mục tiêu lên CD20, một kháng nguyên bề mặt của tế bào B. Nó làm việc bằng cách diệt tế bào B bình thường và gây bệnh và gần đây được sử dụng với thành công lớn để ức chế tổng hợp cryoglobulin. Cyclophosphmide cũng làm giảm tổng hợp cryoglobulin; steroid tiêm tĩnh mạch được đưa vào điều trị để thúc đẩy điều trị viêm cầu thận, và thay huyết tương đã được sử dụng để giảm cryoglobulin tuần hoàn và sau đó làm giảm lắng đọng phức hợp miễn dịch trên thận.
Ở bệnh nhân suy thận tiến triển nhanh hoặc bùng phát cryoglobulin máu cấp, kiểm soát bệnh bằng thuốc ức chế miễn dịch, có hoặc không có thay huyết tương (3 lít huyết tương 3 lần hàng tuần tỏng 2 – 3 tuần), nên được cân nhắc trước hoặc đồng thời với điều trị DAA. Các phác đồ có khả năng gồm rituximab (375 mg/m2 hàng tuần trong 4 tuần, hoặc 2 liều 1g với khoảng cách 14 ngày) có hoặc không có corticosteroid (xem dưới) hoặc cyclophosphamide (2 mg/kg/ngày, điều chỉnh theo GFR, trong 2 – 4 tháng) cộng với methylprednisolone tĩnh mạch 0.5 đến 1 g/ngày trong 3 ngày. Tuy nhiên, các thử nghiệm gần đây ưu tiên hơn cho sử dụng rituximab có hoặc không có steroid so với các phác đồ ức chế miễn dịch trước đây như cyclophosphamide hoặc azathioprine.326-328 Điều quan trọng, nếu phối hợp rituximab với thay huyết tương, thuốc nên sử dụng sau thay huyết tương và vài ngày trước khi thay huyết tương lần sau. Một tùy ý điều trị của các nhà lâm sàng, một phác đồ ức chế miễn dịch đơn độc hoặc phối hợp điều trị DAA được đề nghị khi tiếp cận ban đầu. Ở bệnh nhân có hội chứng thận hư, điều trị ức chế miễn dịch được thêm vào điều trị DAA nên được cân nhắc ở bệnh nhân có biến chứng liên quan đáng kể như bệnh đông máu, giảm albumin máu nặng hoặc anasarca, … Protein niệu trong khoảng thận hư (protein niệu > 3.5 g/ngày) đơn độc không cảnh báo phải dùng ức chế miễn dịch, bệnh nhân đó có thể đạt được sự thuyên giảm protein niệu sau điều trị DAA.295 Đến kỷ nguyên DAA, điều trị phối hợp với corticosteroid và các thuốc ức chế miễn dịch (như điều trị sử dụng tuần tự cyclophosphamide và azathioprine) được sử dụng trong khi đợi đáp ứng, nếu có, với điều trị kháng virus dựa trên IFN. Tiếp cận này thông thường được sử dụng bởi tiên lượng kém của cryoglobulin máu hỗn hợp liên quan đến HCV có GN với điều trị dựa trên IFN đơn độc.309 Tuy nhiên, tiên lượng tốt hơn với DAA và/hoặc rituximab, chúng tôi đề nghị mạnh rằng các phác đồ ức chế miễn dịch cũ chỉ nên được sử dụng nếu rituximab không sẵn có hoặc giá thành quá cao.
| 5.2.3 |
Chúng tôi khuyến cáo điều trị ức chế miễn dịch ở bệnh nhân viêm cầu thận liên qua HCV hoạt động trên mô bệnh học những người mà không đáp ứng với điều trị kháng virus, đặc biệt người có bệnh thận cryoglobuline máu (1B). |
|
| 5.2.3.1. |
Chúng tôi khuyến cáo rituximab là lựa chọn điều trị ức chế miễn dịch đầu tay (1C). |
|
Điều trị ức chế miễn dịch thường dành riêng cho bệnh nhân cryoglobuline máu liên quan đến HCV với biểu hiện bệnh nặng, như bệnh cầu thận tiến triển. Ngoài thuốc ức chế miễn dịch thông thường, mà mục tiêu viêm ở cầu thận, các kết quả đáng khích lệ thu được với điều trị rituximab, một kháng thể đơn dòng chimeric chuột – người, liên kết với kháng nguyên bề mặt CD20 trên tế bào B và chọn lọc tế bào B mục tiêu.326-331 Rituximab ngăn cản tổng hợp cryoglobulin, IgM đơn dòng, và lắng đọng phức hợp miễn dịch tại thận. Một hình thái bệnh lý quan trọng của cryoglobulin máu (bao gồm GN cryoglobulin máu) là kích thích mạn tính của lympho B bởi HCV và mở rộng tổng hợp tự kháng thể liên quan với giảm ngưỡng kích hoạt tế bào do HCV.
Hai RCT đã chứng minh tính vượt trội của rituximab điều trị đơn độc so sánh với điều trị ức chế miễn dịch thông thường (như, corticosteroid, azathioprine, cyclophosphamide, methotrexate, và thay huyết tương) đối với điều trị viêm mạch máu cryoglobulin máu liên quan đến HCV ở bệnh nhân thất bại hoặc không đạt được tiêu chuẩn điều trị IFN. Tuy nhiên, điều quan trọng, chỉ một phần nhỏ bệnh nhân có tổn thương thận.326,328 Rituximab dung nạp tốt và hiệu quả ở 71% đến 83% bệnh nhân viêm mạch máu cryoglobulin máu liên quan đến HCV. Tần xuất tái phát có thể xảy ra sau khi kết thúc điều trị rituximab khi tế bào B hồi ứng lại cấp tính từ máu ngoại vi; ngoài ra, điều trị nhắc lại rituximab tĩnh mạch có thể phơi nhiễm bệnh nhân với nhiều nhiễm trùng cơ hội.
Một nghiên cứu đơn trung tâm, tiến cứu gần đây, rituximab dùng cho 31 bệnh nhân (27 bệnh nhân anti-HCV dương tính) có cryoglobulin máu hỗn hợp (tuýp II ở 29 đối tượng và tuýp III ở 2 đối tượng) và MPGN lan tỏa (n = 16 trường hợp), bệnh thần kinh ngoại vi (n=26 trường hợp) và loét da nặng (n = 7 trường hợp). 5 bệnh nhân được dùng đường tính mạch 500 mg methylprednisolone. Không thêm thuốc ức chế miễn dịch hoặc kháng virus. Thuyên giảm hoàn toàn các triệu chứng hoạt động trước điều trị đã quan sát được ở bệnh nhân tổn thương ban xuất huyết và loét viêm mạch máu không liền, và 80% bệnh thần kinh ngoại vi. 16 bệnh nhân bệnh thận cryoglobulin máu (MPGN lan tỏa và cryoglobulin máu hỗn hợp) những người mà kháng thể HCV dương tính nhận được rituximab ở liều 375 mg/m2, theo liệu trình “4 + 2” (ngày 1, 8, 15, và 22, cộng với một liều sau 1 đến 2 tháng). Tính an toàn và hiệu quả của rituximab được đánh giá trong một khoảng thời gian theo dõi dài (trung bình 72.5 tháng). Một sự cải thiện đáng kể của GN cryoglobulin máu đã quan sát thấy, bắt đầu từ tháng thứ hai sau dùng rituximab (thay đổi creatinin huyết thanh từ 2.1 ± 1.7 mg/dl [186 ± 150 mmol/l] xuống 1.5 ± 1.6 mg/dl [133 ± 141 mmol/l], P < 0.05; thay đổi sau protein niệu 24 giờ từ 2.3 ± 2.1 xuống 0.9 ± 1.9 g/24 h, P < 0.05).327 Sau hai tháng điều trị rituximab, đã ghi nhận sự cải thiện của C4 bổ thể huyết thanh và cryocrit. Không ghi nhận tác dụng phụ lâm sàng liên quan nào. Tái sử dụng rituximab thực hiện ở 9 (trong 31) bệnh nhân tái phát sau trung bình 31.1 tháng (trung vị 55 tháng) sau liệu trình rituximab, do biến cố tim mạch (tuổi trung bình 75.3). Tỷ lệ bệnh không hoạt động sau dùng liều rituximab thứ nhất là 65% ở thời điểm 5 năm, và 50% 5 năm sau lần thứ hai do tái phát.
Một điểm quan trọng cần chú ý rằng rituximab, chọn lọc trên tế bào B mục tiêu, liên quan với biến chứng nhiễm trùng nặng gồm tái hoạt động của HCV,332 nhưng thông thường hơn với HBV. Nguy cơ tái hoạt động của nhiễm HBV được FDA năm 2013 đưa thêm quy định vào cảnh báo “Hộp đen” trên nhãn của rituximab.333 Nhiễm trùng nặng sau khi dùng rituximab đã được quan sát ở người nhận thận ghép và trong cả bối cảnh không ghép tạng.334 Một sự công nhận rằng, các biến chứng đó hầu hết quan sát thấy ở bệnh nhân điều trị phối hợp nhiều thuốc ức chế miễn dịch. Nhiễm trùng thường được báo cáo ở phân nhóm đối tượng cảm nhiễm cao (tuổi > 70, GFR < 60 ml/phút/1.73m2, và dùng đồng thời liều cao corticosteroid) và tử vong ở một số bệnh nhân.335 Bệnh gan ứ mật gây tử vong do tái hoạt động HCV sau một liều rituximab đã được quan sát sau ghép thận.332
Ngoài các thuốc điều trị ức chế miễn dịch thông thường hoặc chọn lọc, các thuốc ức chế miễn dịch khác như MMF có thể cần được đánh giá thêm. Bằng chính chủ yếu đề nghị rằng MMF có thể hiệu quả cho duy trì sự thuyên giảm của GN cryoglobulin máu liên quan HCV.336,337
Tổng hợp lại, bệnh nhân có các loại GN liên quan HCV nhẹ hoặc trung bình với chức năng thận ổn định mà không có hội chứng thận hư nên được quản lý đầu tiên với phác đồ DAA. Bệnh nhân cryoglobulin máu nặng hoặc bệnh cầu thận nặng do HCV (như hội chứng thận hư với các biến chứng liên quan hoặc GN tiến triển nhanh) nên được điều trị với thuốc ức chế miễn dịch (ưu tiên rituximab như một thuốc lựa chọn đầu tay) và/hoặc thay huyết tương thêm vào liệu trình DAA. Bệnh nhân GN liên quan HCV không đáp ứng hoặc dung nạp với thuốc kháng virus nên được điều trị với thuốc ức chế miễn dịch. Các yếu tố thể hiện trên lâm sàng rằng GN liên quan ức chế miễn dịch đáp ứng với điều trị kháng virus bao gồm cải thiện đái máu, mức độ protein niệu, và GFR ổn định (hoặc cải thiện). Do đó, trong nhiều trường hợp, đạt được SVR sau điều trị DAA, thay đổi chức năng thận, hồi phục protein niệu và đái máu, và tác dụng phụ từ điều trị kháng virus phải được theo dõi cẩn thận. Cuối cùng, điều trị tiêu chuẩn protein niệu CKD nên được thực hiện. Bao gồm kiểm soát huyết áp tối ưu, thường xuyên với nhiều loại thuốc bao gồm cả lợi tiểu.315 Ngoài ra, ức chế men chuyển angiotensin hoặc chẹn thụ thể angiotensin nên được sử dụng để điều trị protein niệu.53
NGHIÊN CỨU KHUYẾN CÁO
– Nhiễm HCV ẩn (phát hiện HCV RNA ở tế bào đơn nhân máu ngoại vi và/hoặc tại huyết thanh sau ly tâm) có thể đóng vai trò trong cơ chế bệnh sinh của bệnh cầu thận ở bệnh nhân HCV RNA âm tính.338 Chúng tôi cần các nghiên cứu cỡ mẫu lớn hơn với công nghệ phù hợp để đánh giá mối tương quan giữa HCV ẩn và bệnh cầu thận.
– Hiệu quả và an toàn của điều trị DAA và/hoặc thuốc ức chế miễn dịch đối với điều trị GN liên quan HCV nên được xác nhận ở những nghiên cứu lâm sàng đối chứng lớn với thời gian theo dõi dài hơn.
– Tiếp cận điều trị kháng virus để điều trị GN liên quan HCV đã cải thiện với các phác đồ không có IFN và phác đồ không có RBV. Thông thường, bệnh nhân GN liên quan HCV nhận được một số lượng cao của các thuốc dùng đồng thời, bao gồm cả thuốc có độc tính. Nguy cơ có thể của tương tác thuốc – thuốc nên được nghiên cứu ở bệnh nhân với GN do HCV.
– Vai trò thuốc ức chế miễn dịch trong quản lý GN liên quan HCV mức độ rất nặng (như hội chứng thận hư nặng, giảm GFR tiến triển nhanh) cần được làm rõ hơn để làm sáng tỏ điều trị DAA thời gian rất ngắn.
– Nhiều câu hỏi về sử dụng rituximab ở bệnh nhân vẫn còn GN HCV dương tính. Rituximab đã được dùng thêm ở bệnh nhân GN HCV cho người DAA thất bại với thuyên giảm trên lâm sàng; nói cách khác, rituximab đã được dùng thêm vào DAA. Ở lĩnh vực này, thời gian và liều tối ưu của rituximab truyền tĩnh mạch đối với tái phát là gì? Vai trò của rituximab như một lựa chọn điều trị đầu tay hoặc thuốc tối ưu cần được xác định thêm.
– Nhiễm trùng nặng sau điều trị rituximab thường diễn ra ở bệnh nhân lớn hơn 50 tuổi, có bệnh thận, và dùng đồng thời liều cao corticosteroid. Những nghiên cứu trong tương lai nên được thực hiện để làm thế nào tránh một cách tốt nhất đối với nhiễm trùng liên quan với các phác đồ ức chế miễn dịch.
| Nội dung trước | Trở lại mục lục | Trở lại mục lục |






